نقاط کوانتوم برای کمک به بیماران دیابتی
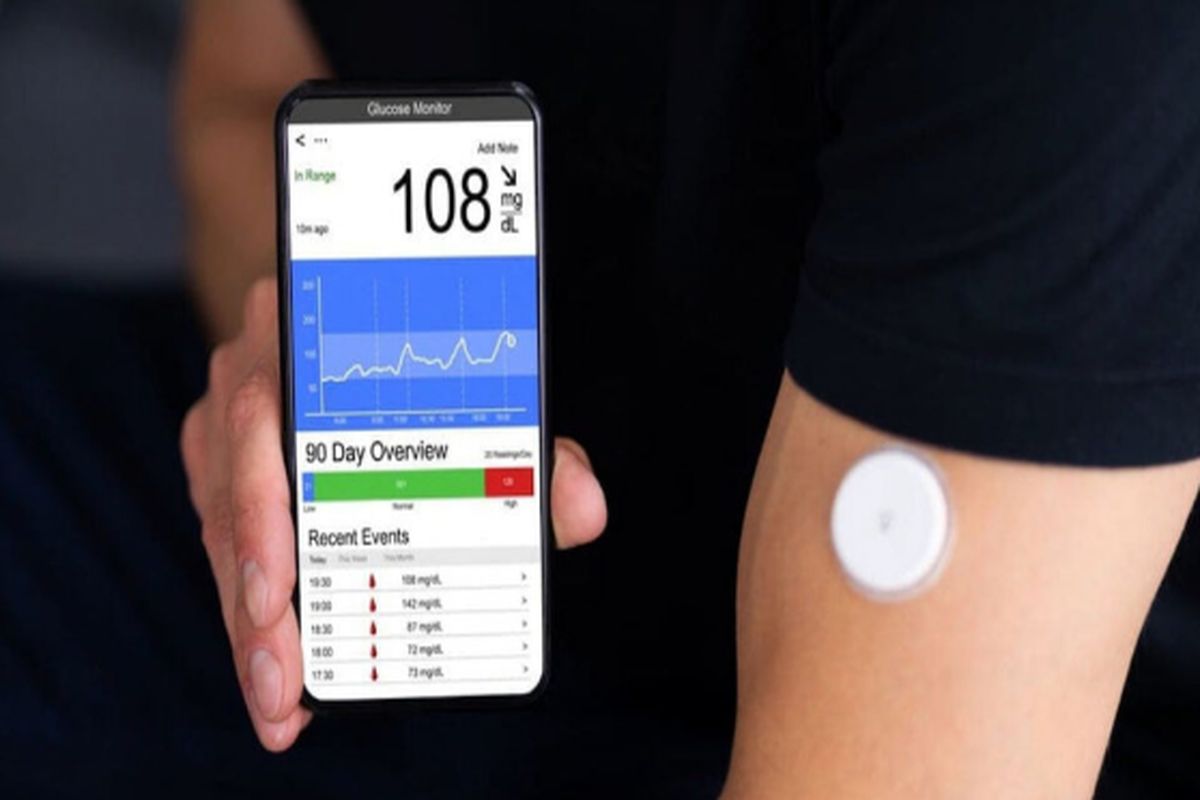
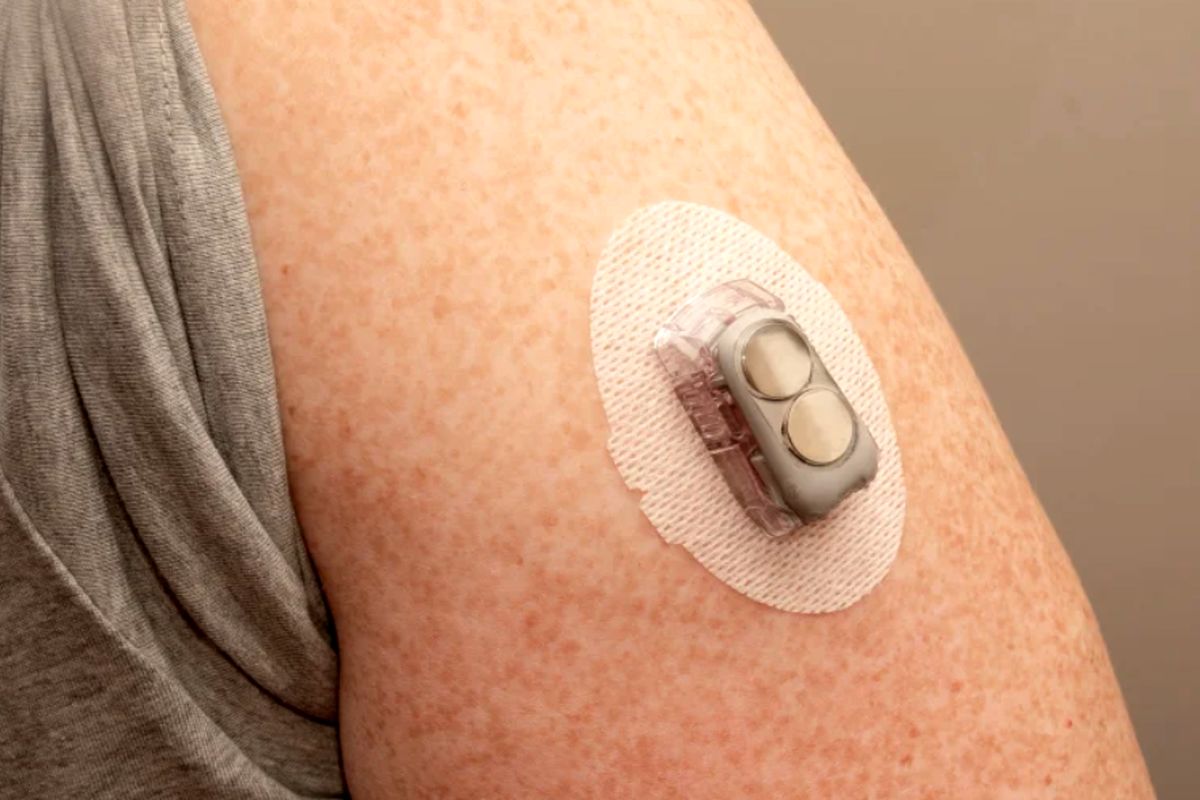
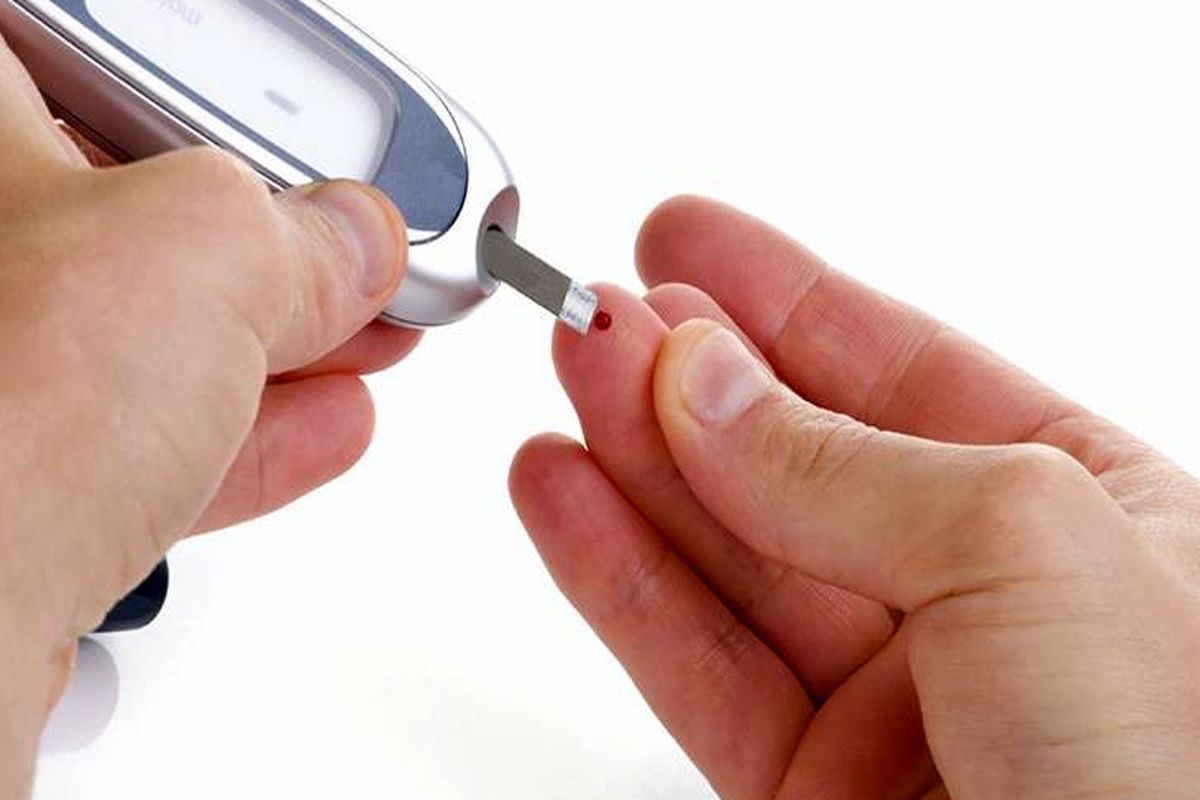
خبرگزاری برنا؛ در سالهای اخیر، توسعه فناوری پایش مداوم گلوکز (CGM) یک ابزار مهم برای افراد مبتلا به دیابت بوده است. برخلاف آزمایش قند خون قبل از غذا و قبل از خواب، تشخیص به موقع، سریع و دقیق سطح گلوکز، دستگاههای CGM بهطور قابل توجهی مدیریت دیابت را بهبود بخشیده است. CGMها معمولاً از طریق یک زیستحسگر کوچک تعبیه شده در زیر پوست کار میکنند که سطح گلوکز را در مایع بین سلولها اندازهگیری میکند. این حسگر هر چند دقیقه یکبار چنین سطوحی را بررسی کرده و اطلاعات را به مانیتور ارسال میکند. مانیتور را نیز میتوان به پمپ انسولین نیز متصل کرد.
روشهای مختلفی از جمله رنگ سنجی، طیفسنجی مادون قرمز، طیفسنجی فلورسانس و طیف سنجی جرمی برای تشخیص گلوکز توسعه یافته است. اما برای کاربرد خانگی و نه در کلینیک یا بیمارستان، تشخیص الکتروشیمیایی گلوکز به دلیل پاسخ سریع، سهولت استفاده، هزینه کم و قابل حمل بودن، پذیرفتهشدهترین روش است.
هونا لیو متخصص میکروالکترونیک در دانشکده اطلاعات نوری و الکترونیکی در دانشگاه علم و فناوری هوژونگ میگوید: «این فناوری دارای حساسیت مناسب است، اما حساسیت عالی ندارد و با سایر روشهای مورد استفاده در یک محیط مراقبتهای بهداشتی مقایسه نمیشود. بنابراین میخواستیم ببینیم که آیا میتوانیم کمی این حساسیت را تقویت کنیم و در نتیجه دقت آن را افزایش دهیم.»
حسگرهای الکتروشیمیایی گلوکز را می توان به دو دسته حسگرهای مبتنی بر آنزیم و حسگرهای غیر آنزیمی طبقهبندی کرد. برای حسگرهای الکتروشیمیایی گلوکز مبتنی بر آنزیم، گلوکز اکسیداز (GOx)، آنزیمی که واکنشهای شیمیایی کاهش اکسیداسیون را تسریع میکند، به طور گسترده برای اکسید کردن گلوکز در سطح الکترود حسگر CGM استفاده میشود. الکترود الکترونها را از گلوکز جذب میکند و در این فرآیند جریان الکتریکی تولید میکند که بسته به سطح گلوکز متفاوت است. GOx به دلیل گزینش پذیری بالا برای گلوکز، پایداری بالا و فعالیت بالا در طیف وسیعی از سطوح pH بهطور گسترده برای این منظور استفاده می شود.
با این حال، هنگامی که GOx مستقیماً با سطح الکترود برهنه ترکیب میشود، نه تنها خود GOx به راحتی لایهبرداری میشود، بلکه فعالیت زیستی و پایداری آن نیز میتواند تحت تأثیر قرار گیرد. علاوه بر این، راندمان انتقال الکترون بین GOx و سطح الکترود یک عامل کلیدی تعیینکننده حساسیت حسگر است.
تاکنون، تلاشهای متعددی برای چسباندن محکمتر آنزیم GOx به الکترود انجام شده و در نتیجه انتقال مستقیم الکترون بین مراکز الکترواکتیو و سطح الکترود افزایش مییابد. یک روش استفاده از الکترودهایی است که در مقیاس نانو طراحی شدهاند تا ساختارهایی بر روی الکترود داشته باشند که سطح بزرگتر و فعالیت الکتروکاتالیستی بالا را فراهم کنند. متأسفانه، این نانوساختارها پیچیدگی ساخت چنین حسگرهای زیستی الکتروشیمیایی را افزایش می دهند. ساختار آنها همچنین به پلیمر مصنوعی Nafion به عنوان یک داربست متکی است، که مانعی برای انتقال بار در سطح رابط بین حسگر و مایع مورد آزمایش ایجاد میکند.
بنابراین محققان به مسیری کاملاً متفاوت رفتهاند. هدف این تیم بهبود عملکرد حسگری گلوکز با استفاده از نقاط کوانتومی کلوئیدی (CQD) بهعنوان مادهای برای اصلاح الکترود بود.
محققان نانوکرههای طلا را در ساختار الکترود حسگر ادغام کردند. این نانوذرات کروی بسیار ریز با قطرهای ۱۰ تا ۲۰۰ نانومتر هستند که به دلیل خواص فیزیکی و شیمیایی منحصر به فردشان بهطور فزایندهای در کاربردهای حسگری زیستی مورد استفاده قرار میگیرند. هنگامیکه بهعنوان یک جزء در حسگرهای زیستی الکتروشیمیایی آنزیمی استفاده میشود، AuNSs به آنزیمهای پروتئینی اجازه میدهد تا فعالیت زیستی خود را پس از چسبیدن به سطوح حفظ کند. در یک CGM، این دامنه سیگنال زیستحسگر الکتروشیمیایی را بسیار افزایش میدهد.
محققان یک CGM اثبات مفهوم را با استفاده از CQDها در این مورد از سولفید سرب و الکترود اصلاح شده با AuNSs ساختند. اکنون قصد دارند CGM اثبات مفهوم خود را توسعه داده و آن را در مقیاس تجاری تولید کنند.
انتهای پیام/